Odhalenie tajomstiev je najúčinnejšie cestou pochopenia jednoduchých a základných princípov. Rovnako môžeme vyjasniť zákernosť, zložitosť a problémový charakter chronických latentných perzistentných infekcií (ďalej v skratke Ch.L.P.I.). Veľmi významný, ak nie najvýznamnejší podiel na uvedených špecifikách Ch.L.P.I. má veľkosť patogénu. Porovnanie relatívnej veľkosti polomeru alebo aspoň približného polomeru rôznych druhov buniek logicky naznačuje správanie patogénnych mikroorganizmov.
Na prehľadom schematickom obrázku je zobrazená veľkosť najväčšej telesnej (somatickej) bunky (cca 200um), najväčšej baktérie (cca 2 um), najmenšieho vírusu (cca 15nm), ako aj akéhosi medzistupňa baktérie a vírusu tzv. parabaktérie (desiatky nm), čo zodpovedá väčšine pôvodcov Ch.L.P.I.
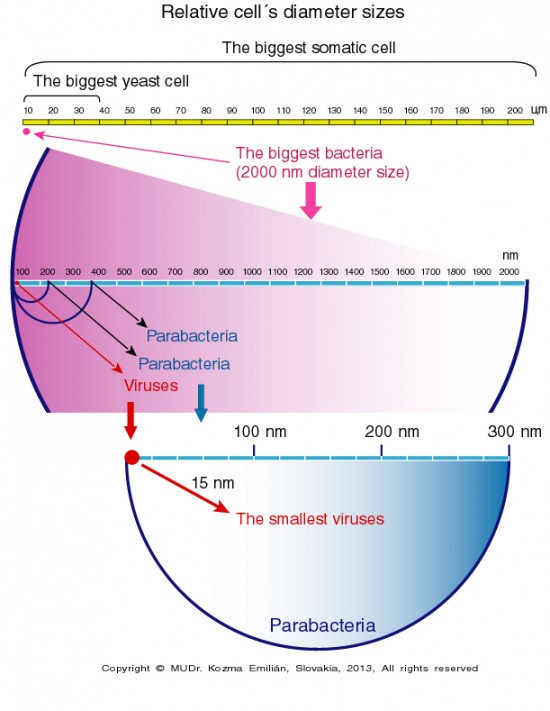
Už samotné mechanické pomery sú predpokladom existencie uvedených patogénov (parabaktérií) vnútri väčších buniek, hlavne somatických. Do úvahy treba zobrať aj vnútrobunkové subštruktúry a mechanické priestorové možnosti pre patogén.
Lokalita uvedených vnútrobunkových (intracelulárnych) patogénov je u rôznych patogénov odlišná čo sa týka vnútrobunkových subštruktúr. Napríklad s.aureus, salmonela, m. leprae sú vnútri bunky lokalizované v tzv. fagolyzozómoch. Tieto skutočnosti musí poznať aj lekár indikujúci liečbu tak, aby liečivo (najmä antibiotika) bolo schopné preniknúť do týchto štruktúr, v danom prípade napr. makrolidy, aminoglykoziky. Legionely a chlamýdie sú napr. lokalizované vo fagozómoch, listérie a shigely v cytozole, kam prenikajú fluorochinolóny, beta laktámy a ansamycíny.
Pre stručné vysvetlenie:
Lyzozóm je degradačnou štruktúrou bunky obsahujúcou kyslé hydrolázy.
Fagozóm je membránovou subštruktúrou bunky s pohltenou baktériou.
Endozóm je transportnou formou subštruktúry bunky, ktorú tvorí súbor organel regulujúcich transport v rámci vnútorného membránového systému (vačok, vezikula). Endozóm je kyslejší ako cytozól a obsahuje manóza-6-fosfátový receptor (MPRs).
Vývojové fázy endozómu sú včasný endozóm (pH 6,5), multivezikulárne teliesko, neskorý endozóm (pH 4,5).
Cytozól je vnútrobunkové tekuté médium tvoriace prostredie pre ostatné subštruktúry bunky.
Donedávna boli kľúčovými poznatkami pri genéze endo-fago-lyzozómov tzv. Rab (G proteín) a Clathrin proteíny.
Rab proteíny hrajú významnú úlohu v regulácii transportných vnútrobunkových procesov vrátane tvorby vezikúl a podobných subštruktúr. Clathrin proteíny hrajú hlavnú úlohu pri tvorbe plášťa vezikúl.
V r. 2008 boli publikované sľubné výskumné výsledky o profiloch stovkách proteínov v membráne fagozómov, ako aj o proteínoch sprostredkujúcich "komunikáciu" medzi imunitným systémom a fagocytózou. Jeden z proteínov LC3-II je považovaný za sľubný marker autofágie, čo je samoočistný proces vnútri bunky.
Tieto poznatky sú kľúčom k efektívnej profesionálnej detoxifikačnej terapii na bunkovej úrovni nevyhnutnej práve pri liečbe Ch.L.P.I.
Aplikácia najnovších poznatkov z uvedených oblastí je nevyhnutnou súčaťou inovatívne orientovanej medicíny, ako aj nevyhnutnosťou pre pochopenie podstaty patogenézy, farmakokinetiky, stratégie a taktiky najnovších terapeutických metód hlavne v klinickej praxi.